Produkte – in Produktgruppen organisiert
Zum leichteren Auffinden einzelner Produkte haben wir unser Lieferprogramm in handliche Produktgruppen untergliedert. Diese werden Ihnen nachfolgend angezeigt. Wählen Sie Ihre gewünschte Produktgruppe aus:
Notfallmedizin





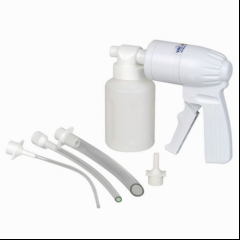
Absaugpumpe Vacq-Breezer
Absaugpumpe



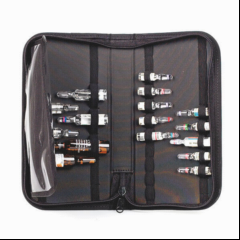
Ampullenetui
Notfallkoffer, Ampullenetui


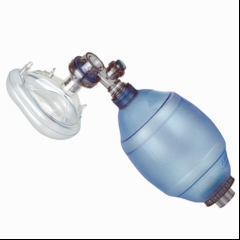
Beatmungsbeutel Blue Line
Beatmungsbeutel




Beatmungsmaske mit Luftwulst
Beatmungsmaske

Chirurgiesauger
Chirurgiesauger





Clearline II PVC-Einwegbeatmungsbeutel
Beatmungsbeutel


Euro Schaufeltrage
Schaufeltrage
Evac+Chair Modell MK4
Evakuierungsstuhl
Leichenhülle ECO
Leichenhülle
Leichenhülle Standard
Leichenhülle
Leichentransport-/ Bergungshülle
Leichentransporthülle


Lifebox 1, Basis, Notfallkoffer
Notfallkoffer


Lifebox 1, DIN 13232, Notfallkoffer
Notfallkoffer


Lifebox 1, Pflegeheim, Notfallkoffer
Notfallkoffer
Lifebox U1 Notfallkoffer, Atmung
Notfallkoffer
Lifebox U2 Notfallkoffer, Basic
Notfallkoffer
Lifebox U3 Notfallkoffer Komplettausstattung
Notfallkoffer
Lifebox U3 Notfallkoffer Typ: Erwachsene
Notfallkoffer
Lifebox U3 Notfallkoffer Typ: Kinder
Notfallkoffer

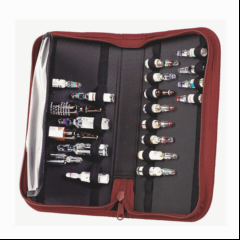
Lifeguard Ampullarium
Ampullarium



Lifeguard elektrische Absaugpumpe LIFETIME Akku
Absaugpumpe




Lifeguard MP-Carrier
Rettungsschlitten

Lifeguard Sanitätsschrank Short
Sanitätsschrank
Lifeguard Schaufeltrage
Schaufeltrage

Lifeguard Verbandschrank Typ 1
Verbandschrank







Max Cases Notfallkoffer
Notfallkoffer
Primedic Heart Save PAD
Defibrillator
Primedic HeartSave 6 (AkuPak Lite)
Defibrillator
Primedic HeartSave AED (Batterie)
Defibrillator

Primedic HeartSave AED-M
Defibrillator










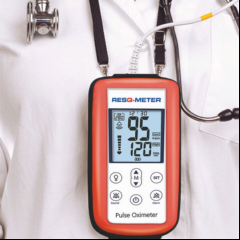
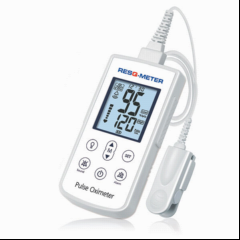
Pulsoximeter RESQ-Meter
Pulsoximeter


Sauerstoffflaschen-Tasche
Sauerstoffflaschen Tasche




SPINEBOARD MIT SPEED-CLIPS
Spineboard
Ulmer Koffer I leer
Notfallkoffer
Ulmer Koffer II leer
Notfallkoffer
Ulmer Koffer III leer
Notfallkoffer








VACQ-BLUE II Vakuummatratze Set
Vakuummatratze

Verbandtasche, fertig gefüllt
Verbandtasche
Zubehör für HeartSave Defis
Defibrillator
Medizinprodukte-Klassifizierung
08.12.2015| Die Klasse eines Medizinprodukts orientiert sich rechtlich an der "Verletzbarkeit des menschlichen Körpers" durch das jeweilige Produkt. Diese wiederum definiert sich über die Zweckbestimmung des Herstellers hinsichtlich des Anwendungsorts und der Anwendungsdauer seines Produkts. Die Medizinprodukte-Klasse bedingt den mit zunehmender Klassenhöhe ebenfalls zunehmenden Anteil an Fremdkontrolle bzw. an (externer) Zertifizierung des Konformitätsbewertungsverfahrens (Verfahren zum Nachweis der Erfüllung aller gesetzlichen Produktanforderungen) durch eine Benannte Stelle.
Kriterien für die Einteilung in 4 Klassen sind:
- Dauer der Anwendung (bis 60 Minuten, bis 30 Tage, länger als 30 Tage)
- Ort der Anwendung: Grad der Invasivität (invasiv, chirurgisch invasiv, implantierbar),
- Anwendung am zentralen Kreislaufsystem oder am zentralen Nervensystem
- Wiederverwendbares chirurgisches Instrument
- Aktives Medizinprodukt (Aktives therapeutisches Medizinprodukt / Aktives diagnostisches Medizinprodukt)
- Verwendung von biologischem Material aus Tieren oder Menschen
Die Klassen sind EU-weit durch den Anhang IX der Richtlinie 93/42/EWG festgelegt:
Klasse I
Keine methodischen Risiken
geringer Invasivitätsgrad
kein oder unkritischer Hautkontakt
vorübergehende Anwendung ≤ 60 Minuten
Klasse IIa
Anwendungsrisiko
mäßiger Invasivitätsgrad
kurzzeitige Anwendungen im Körper (im Auge, intestinal, in chirurgisch geschaffenen Körperöffnungen)
kurzzeitig ≤ 30 Tage, ununterbrochen oder wiederholter Einsatz des gleichen Produktes
Klasse IIb
Erhöhtes methodisches Risiko
systemische Wirkungen
Langzeitanwendungen
nicht invasive Empfängnisverhütung
langzeitig ≥ 30 Tage, sonst wie bei kurzzeitig
Klasse III
entspricht hohem Gefahrenpotential
Besonders hohes methodisches Risiko
zur langfristigen Medikamentenabgabe
Inhaltsstoff tierischen Ursprungs und im Körper
unmittelbare Anwendung an Herz, zentralem Kreislaufsystem oder zentralem Nervensystem
und natürlich invasive Empfängnisverhütung
Für die Bewertung von Risiken gilt bei Einhalten der harmonisierten Norm ISO 14971:2007 die Konformitätsvermutung. Wird diese Norm nicht eingehalten, ist die Gleichwertigkeit der gewählten Lösung mit der harmonisierten Norm nachzuweisen.
Die Regeln zur Klassifizierung sind detailliert im Anhang IX der EU-Richtlinie 93/42/EWG festgelegt. Die Anwendung der Klassifizierungsregeln richtet sich nach der Zweckbestimmung der Produkte (und liegt daher in der Verantwortung des Herstellers).
Einige konkrete Beispiele für Medizinprodukte sind:
Klasse I
ärztliche Instrumente
Gehhilfen
Rollstühle
Pflegebetten
Stützstrümpfe
Verbandmittel
wiederverwendbare chirurgische Instrumente
OP-Textilien
Klasse IIa
Dentalmaterialien, Dentalimplantate
Desinfektionsmittel (für Instrumente und Geräte)
diagnostische Ultraschallgeräte
Einmalspritzen
Hörgeräte
Kontaktlinsen
PACS
Trachealtuben
Zahnkronen
Klasse IIb
Anästhesiegeräte
Beatmungsgeräte
Bestrahlungsgeräte
Blutbeutel
Defibrillatoren
Dialysegeräte
Kondome
Kontaktlinsenreiniger
Reinigungsdesinfektionsautomaten
Klasse III
Herzkatheter
künstliche Hüft-, Knie-, oder Schultergelenke
Stents
resorbierbares chirurgisches Nahtmaterial
Intrauterinpessar (Spirale)
Brustimplantat
Herzschrittmacher
Es ist jedoch zu beachten, dass weder durch die EU-Richtlinien noch durch die nationale Gesetzgebung eine derartige Klassifizierung von Medizinprodukten vorgenommen wird, da jeweils im Einzelfall, bezugnehmend auf den bestimmungsgemäßen Gebrauch (“intended use”), die Klassifizierung durchzuführen ist.
Eine detaillierte Orientierungshilfe für die Klassifizierung von Medizinprodukten bietet der Leitfaden "Klassifizierungsliste Medizinprodukte" aus der BVMed-Informationsreihe "Medizinprodukterecht".
Definition Medizinprodukte
10.10.2016| Medizinprodukt bezeichnet einen Gegenstand oder einen Stoff, der zu medizinisch therapeutischen oder diagnostischen Zwecken für Menschen verwendet wird, wobei die bestimmungsgemäße Hauptwirkung im Unterschied zu Arzneimitteln primär nicht pharmakologisch, metabolisch oder immunologisch, sondern meist physikalisch oder physikochemisch erfolgt. Die Abgrenzung der Medizinprodukte zu Arzneimitteln ist bedeutsam, da Marktzugang und Verkehrsfähigkeit unterschiedlich geregelt sind.
In Deutschland regelt das Gesetz über Medizinprodukte (Medizinproduktegesetz - MPG) vom 2. August 1994 den Verkehr mit Medizinprodukten. Es dient der nationalen Umsetzung von drei europäischen (Stamm-) Richtlinien (90/385/EWG [aktive implantierbare medizinische Geräte], 93/42/EWG [sonstige Medizinprodukte] und 98/79/EG [In-vitro-Diagnostika]), die durch spätere Änderungsrichtlinien ergänzt bzw. geändert wurden, zuletzt mit Richtlinie 2007/47/EG vom 5. September 2007 zum 21. März 2010. Das MPG und seine acht ausführenden Rechtsverordnungen enthalten darüber hinaus weitere nationale Regelungen, die hauptsächlich der Überwachung im Markt befindlicher Medizinprodukte (Marktüberwachung) dienen.
§ 3 MPG enthält in Nr. 1 bis 4 die Legaldefinition/en des Begriffs Medizinprodukt:
Medizinprodukte sind alle einzeln oder miteinander verbunden verwendeten Instrumente, Apparate, Vorrichtungen, Software, Stoffe und Zubereitungen aus Stoffen oder andere Gegenstände einschließlich der vom Hersteller speziell zur Anwendung für diagnostische oder therapeutische Zwecke bestimmten und für ein einwandfreies Funktionieren des Medizinproduktes eingesetzten Software, die vom Hersteller zur Anwendung für Menschen mittels ihrer Funktionen zum Zwecke
a) der Erkennung, Verhütung, Überwachung, Behandlung oder Linderung von Krankheiten,
b) der Erkennung, Überwachung, Behandlung, Linderung oder Kompensierung von Verletzungen oder Behinderungen,
c) der Untersuchung, der Ersetzung oder der Veränderung des anatomischen Aufbaus oder eines physiologischen Vorgangs oder
d) der Empfängnisregelung
zu dienen bestimmt sind und deren bestimmungsgemäße Hauptwirkung im oder am menschlichen Körper weder durch pharmakologisch oder immunologisch wirkende Mittel noch durch Metabolismus erreicht wird, deren Wirkungsweise aber durch solche Mittel unterstützt werden kann.
Anders als Arzneimittel sind Medizinprodukte hauptsächlich physikalisch wirkende Gegenstände. Bei den meisten Medizinprodukten ist der Nutzen direkt ersichtlich. Es ist zudem Teil des Zulassungsverfahrens (Konformitätsbewertung), dass das Medizinprodukt seine vom Hersteller vorgesehene Zweckbestimmung erfüllt. Dabei geht es vor allem um den Nachweis der Sicherheit und Leistungsfähigkeit der Produkte.